Formules Spatiales
Avant
d'entrer dans le "vif du sujet", nous allons dans cette rubrique
vous expliquer la représentation de Cram et la projection de Newman
qui nous permettront par la suite d'expliquer pourquoi les molécules
peuvent ou non être définies comme chirales.
D'autres formules spatiales
existent, mais ici nous ne parlons que de ces deux là.
. Représentation de Cram
La
représentation plane d'une structure tridimensionnelles n'est pas chose
facile. Aussi a -t-on l'habitude de représenter les liaisons selon
les conventions suivantes, dites de Cram :
Un
trait plein représente une liaison entre deux atomes situés
dans le plan de la figure.
Les angles entre les liaisons ainsi représentés sont respectés.
Un triangle allongé plein représente une liaison entre un atome
situé dans le plan de la figure (à la pointe du triangle) et
un atome situé en avant de ce plan (à la base du triangle).
Un triangle allongé hachuré ou un pointillé représente
une liaison entre un atome situé dans le plan de la figure (à
la pointe) et un atome situé à l'arrière de ce plan (à
la base)

. Projection de Newman
Construisons
un modèle éclaté de la molécule d'éthane,
et repérons les atomes de carbone par les lettres grecques alpha et
béta.
Bloquons l'un des groupes méthyle, par exemple CbétaH3 : il
constitue le solide de référence.
Faisons tourner le second groupe, noté CbétaH3, autour de l'axe
Calpha-Cbéta.
La molécule passe ainsi par une infinité de structures appelées
conformations.
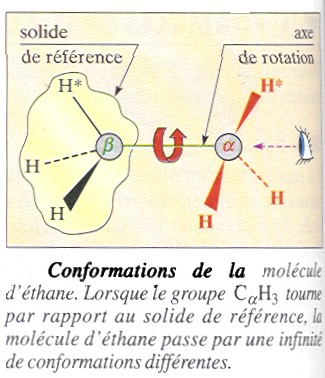
On
appelle conformations d'une molécule les différentes structures
spatiales qu'elle peut prendre par suite de rotations autour de ses liaisons
simples.
La visualisation des différentes conformations obtenues par rotation
autour d'une simple liaison est grandement facilitée par l'utilisation
de la projection de Newman.
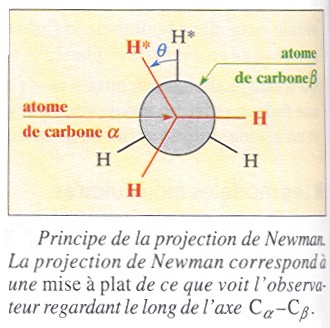
On dispose la molécule d'éthane de manière à ce que les atomes d'hydrogène de deux groupes CH3 se trouvent exactement les uns en face des autres : cette conformation est dite éclipsée, car si nous représentons en projection de Newman la molécule le long de l'axe Calpha-Cbéta, les atomes d'hydrogènes portés par Cbéta sont masqués, éclipsés par ceux que portent Calpha
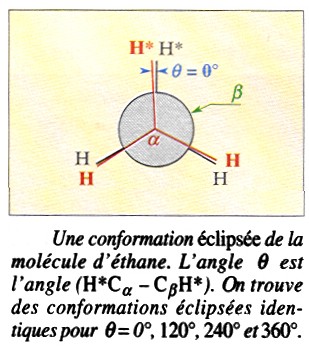
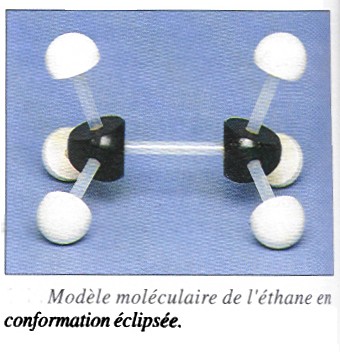
On
marque deux atomes d'hydrogène d'un astérisque et on définit
l'angle téta. Lorsque téta croît de 0° à 60°,
la molécule passe continûment par une infinité de conformations,
toutes différentes.
Pour téta=60°, elle se trouve dans une conformation remarquable
appelée conformation décalée
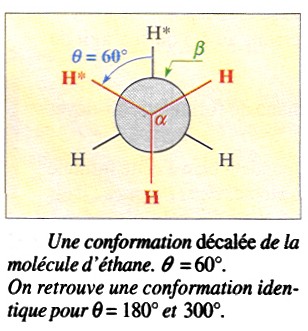

Lorsque
téta croit de 60° à 120°, la molécule retrouve
les mêmes conformations que dans l'intervale [0°,60°], mais
dans l'ordre inverse. Pour téta=120°, nous obtenons une conformation
éclipsée identique à la conformation initiale (téta=0°)